慢性病性贫血(anemia of chronic disease ,ACD),亦称作炎症相关性贫血(Anemia of inflammation,AI),是最常见的贫血之一。
病因
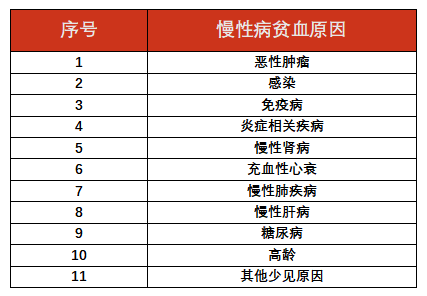
表1:慢性病贫血病因
发病机制
慢性病贫血发生机制复杂,如图1:
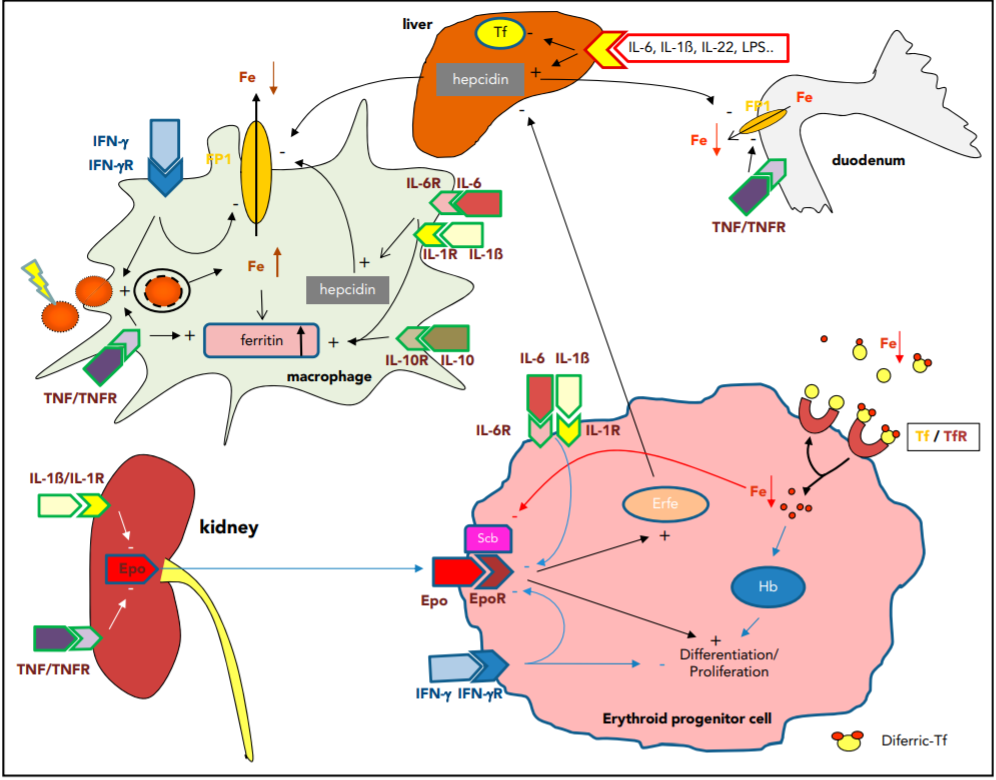
图一:慢性病贫血发生机制
铁利用受限
慢性病患者处于持续免疫激活状态,细胞因子(如IL-6,IL-1β,IL-22,TNF等),微生物产物,自身抗原,肿瘤相关抗原等的释放,通过调节铁调素、转铁蛋白等的生成,一方面导致肠道铁吸收减少,另一方面影响铁转运及储存,使铁滞留在网状内皮系统中。而铁为红细胞生成所必须,循环铁大于90%均来自网状内皮系统,铁的循环受限导致红细胞生成原料缺乏,进而导致贫血。
红细胞生成受抑
细胞因子及自由基能抑制Epo、EpoR的生成,直接损伤肾上皮细胞,红系前体细胞,诱导细胞凋亡,从而抑制红细胞生成。
红细胞寿命减短
红细胞表面抗体、补体沉积,微血管纤维蛋白原沉积,同时巨噬系统激活,均导致红细胞更易被巨噬细胞吞噬,导致红细胞寿命减短。
诊断
女性Hb<120g/L,男性Hb<130g/L,同时有铁代谢稳态改变,炎症活动的临床/实验室证据即可诊断,但需同时寻找合并的其他需要特殊治疗的因素,如出血、溶血、药物、营养性贫血等。
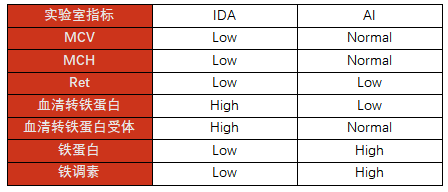
慢性病贫血通常表现为正色素,正细胞性贫血,血清铁、转铁蛋白饱和度、转铁蛋白减低,铁蛋白正常或升高。但部分AI患者可能同时合并隐性失血导致的缺铁性贫血(IDA),此类患者有时难以鉴别,此时铁调素测定可能有助于鉴别。AI/IDA患者需积极寻找隐形出血部位,以对症处理。
表2:缺铁性贫血与炎症相关贫血实验室指标差异
治疗
病因治疗:
病因治疗是慢性病贫血治疗的基石。
输血:
血细胞输注存在许多副反应,如过敏,溶血,肺水肿,感染,铁过载等问题,因此输血需遵循“less is more”的原则,尽量减少输血,仅推荐用于重度贫血、临床急需纠正缺氧状态或存在活动性大出血时。
红细胞生成刺激剂(erythropoiesis-stimulating agents,ESA):
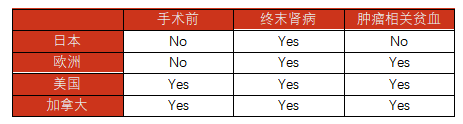
ESA治疗存在争议,部分研究显示,ESA会增加短期死亡率,可能因为ESA短期无法显示疗效,但会增加血栓生成及血管新生。不同国家及地区对ESA的使用有不同推荐,具体见表3。
表3:不同地区对ESA治疗AI的推荐
补铁治疗
通过实验室检查评估患者的铁缺乏程度,对于存在铁缺乏的患者,可给予口服/静脉补铁治疗,如图2:
图2:铁缺乏评估及治疗推荐

其他
铁调素抑制剂,脯氨酰羟化酶抑制剂等均在临床试验中显示出一定疗效。
图3:AI新药相关临床试验
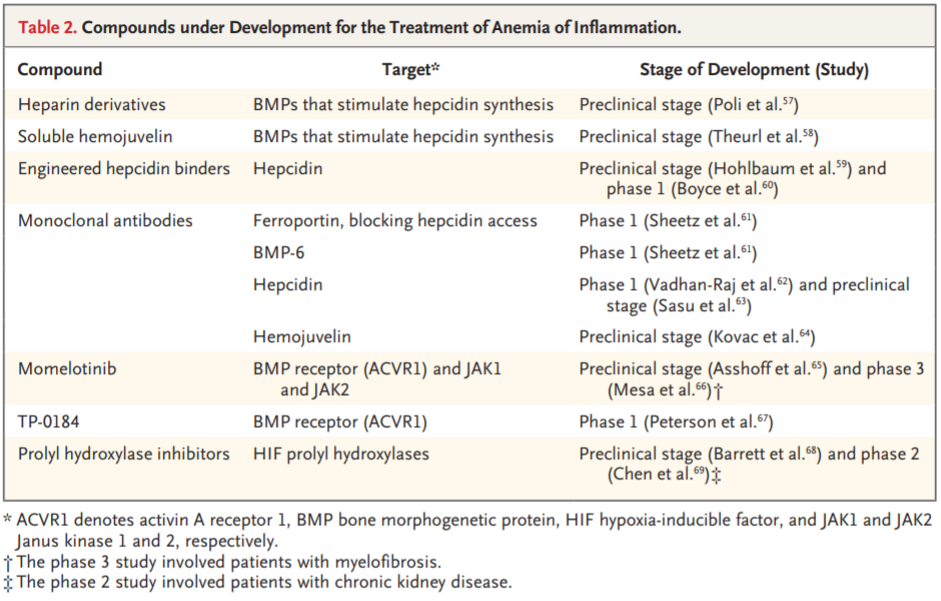
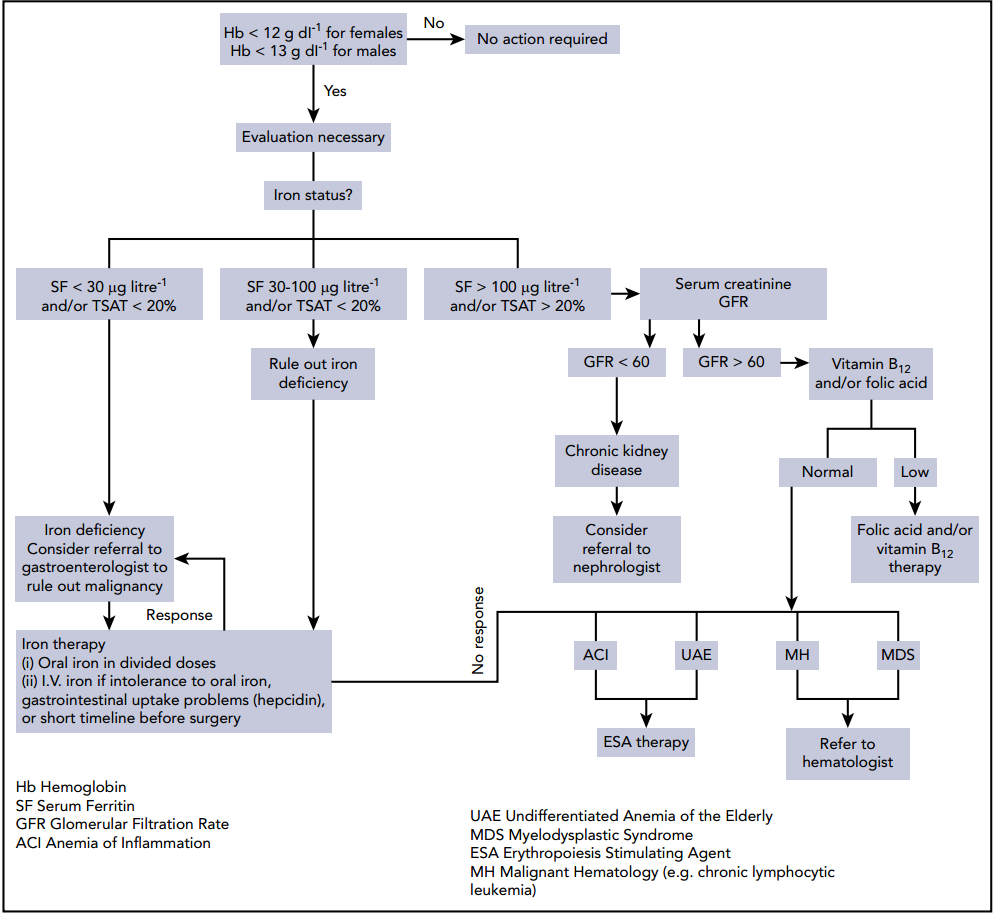
图4:贫血诊治流程
参考文献
1. Weiss, G., T. Ganz, and L. Goodnough, Anemia of inflammation. Blood, 2019. 133(1): p. 40-50.
2. 肿瘤相关性贫血临床实践指南(2015-2016版). 中国实用内科杂志.2015,35(11):921-930.
3. Ganz, T., Anemia of Inflammation. The New England journal of medicine, 2019. 381(12): p. 1148-1157.

