
人体免疫系统的主要功能就是区分自体与外来物,从而保护机体健康。但肿瘤对免疫系统而言是一个独特的挑战,它来源于机体自身细胞,免疫系统难以识别;此外肿瘤构建的微环境对免疫反应的抑制也让T细胞难以发挥杀伤功能。
近年来,通过基因工程改造的T细胞作为“活的药物”消灭癌细胞是肿瘤治疗的一个新方向。目前,使用表达嵌合抗原受体(CAR)的T细胞(CART)和转基因T细胞受体的T细胞(TCR-T)在治疗恶性肿瘤的临床试验中表现出了惊人的疗效。
01
T细胞的激活或抑制
T细胞受体(TCRs)为所有T细胞表面的特征性标志,以非共价键与CD3结合,形成TCR-CD3复合物。TCR是由2条不同肽链构成的异二聚体,每条肽链均由可变区,恒定区,跨膜区与胞质区组成,其胞质区很短。TCR的主要功能是识别由MHC I类或II类分子提呈的抗原肽。CD3是一种跨膜蛋白,主要功能是参与TCR-CD3复合体的装配和稳定以及信号转导(图1)。
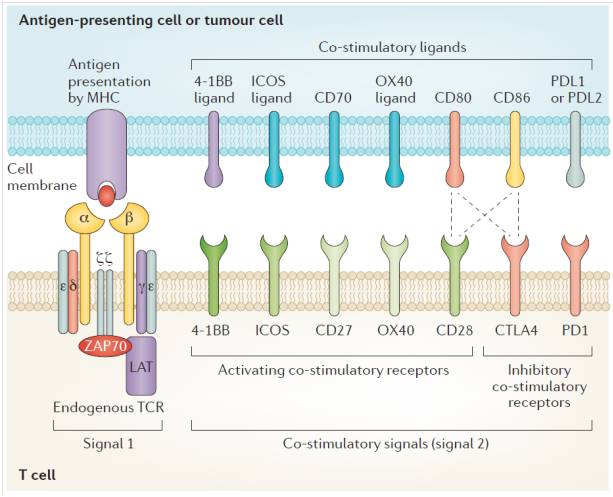
图1.TCR与共刺激信号
T细胞杀伤肿瘤细胞的前提是被激活并增殖,此过程需要两条细胞信号通道共同作用,一是TCR与MHC提呈的抗原肽结合(信号1),激活T细胞;二是T细胞的CD28或4-1BB等表面蛋白与其受体相结合形成共刺激信号(信号2),刺激T细胞增殖。当TCR-MHC-抗原肽第一信号与共刺激信号共同存在时,ζ链很快发生酪氨酸磷酸化,激活细胞内信号传导途径,使细胞骨架蛋白改变以及核内转录因子活化,引起T细胞的激活并增殖。
02
肿瘤细胞逃逸的机制之一:抑制T细胞激活与下调MHC分子表达 MHC抗原提呈机制与共刺激机制确保了杀伤力强大的T细胞进行特异性识别,但同时也让肿瘤细胞形成了一种逃逸机制。肿瘤细胞在不断的发生发展过程中,逐渐适应体内的免疫环境,下调MHC分子的表达,甚至不再表达MHC。这将导致T细胞不能识别肿瘤细胞,造成肿瘤细胞免疫逃逸,继续恶化。另外,CTLA4与PD-1是典型的共刺激抑制信号。 CTLA4与其配体CD86结合后,可抑制T细胞的活化;而且许多肿瘤细胞通过上调PD1配体——PDL1或PDL2的表达来阻止T细胞的激活。
03 基因工程T细胞(TCR-T、CART) 结构比较 通过转基因方法在T细胞中表达的TCR(TCR-T)与T细胞本身表达的TCR在结构上没有明显的区别。主要区别是转基因方法在T细胞中表达的TCR已经过人工筛选,可以与MHC分子提呈的肿瘤抗原相结合。但是TCR-T细胞仍然需要同时被信号2刺激才能被完全激活,仍然会受到PD-L1等抑制免疫反应的蛋白抑制。 而CART表面的CAR分子将识别肿瘤抗原的抗体片段与TCR-CD3复合物的胞内域和接受共刺激信号的受体的胞内域嵌合在一起,这种受体不需要MHC的辅助就可以识别肿瘤表面抗原,同时也不需要肿瘤细胞表面的信号2,就可以激活T细胞(图2.)。
图2. 基因工程T细胞结构比较
04 CART技术的基本原理 CART,又名嵌合抗原受体T细胞。治疗流程是从人外周血分离出T细胞,在体外进行基因修饰,增强其对肿瘤细胞的识别能力,扩增培养到一定数量后,回输患者。其中,在体外进行基因修饰环节是CART的核心技术。将设计好的CAR基因转入T 细胞的基因组中,T细胞就可以表达相应的CAR结构(嵌合抗原受体)。CAR结构将使T细胞越过MHC抗原提呈机制直接识别肿瘤细胞,同时获得共刺激信号,被“一键激活”。即CAR结构是将抗体中可以直接识别肿瘤抗原的可变单链区域scFv(抗原受体)、共刺激信号都嵌合到T细胞的激活信号通路CD3ζ链上(图3.)。利用抗原-抗体机制,CART细胞可以直接识别肿瘤细胞表面抗原,相当于采用“人脸识别系统”来替代“检查身份证”的MHC抗原提呈机制,肿瘤细胞就不能通过下调MHC来逃避CART细胞的追杀了。同时CAR结构中形成了“识别-共刺激-激活”的信号转导通路,所以当抗体部分识别了肿瘤细胞表面抗原时,T细胞同时获得了信号1又有信号2,可以被一键激活。
图3. CART细胞利用抗原抗体机制直接识别肿瘤抗原(非MHC限制性) CART技术的三大优势:一、非MHC限制性;二、可识别抗原种类多,MHC只能提呈蛋白质片段(多肽),而CAR的抗原抗体机制可以识别细胞表面的蛋白质、多糖,以及脂类蛋白,应用较为广泛;三、CART可在体内继续增殖为“活的药物”,形成持续的杀伤力,而且还可以释放细胞因子召集更多的免疫细胞协同作战。
05 CAR结构的演变
CAR自从出现以来,它的结构经过了多次改进。第一代的CAR的胞内域只有一个媒介TCR信号的CD3ζ片段,缺乏协同刺激信号,T细胞增殖能力弱。而第二代的CAR的胞内域添加了协同刺激信号的CD28或4-1BB片段,T细胞在体内可增殖数百倍。而第三代则在胞内域部分整合了3或4种共刺激信号的受体片段,从而使激活效率变得更高,在体内存续时间长。(图4.) 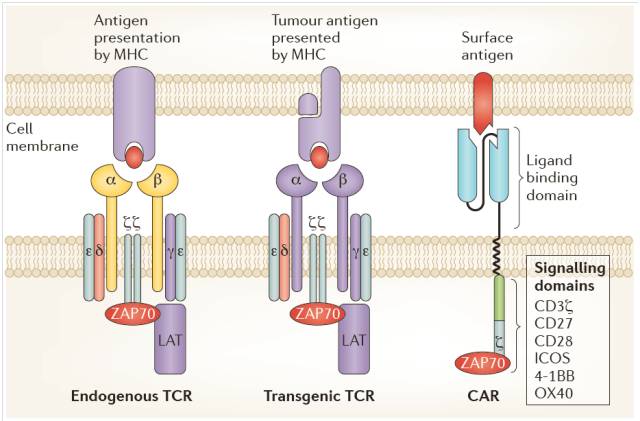
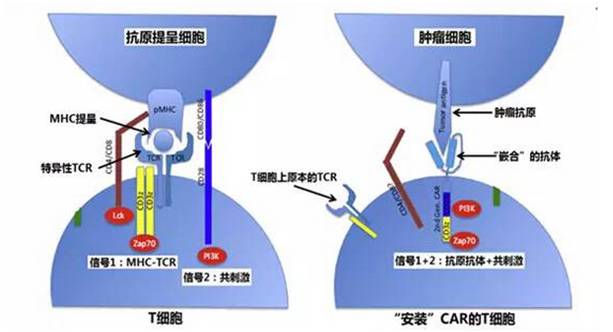
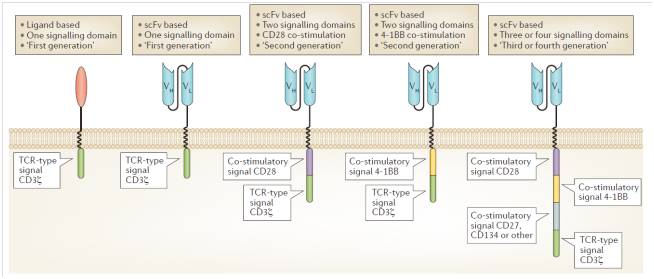
图4. CAR结构演变

