抗中性粒细胞胞浆抗体(ANCA)相关性血管炎(AAV)是一种严重的自身免疫性疾病,主要影响血管壁,导致炎症、坏死和血管狭窄。AAV包括肉芽肿性多血管炎(GPA)、显微镜下多血管炎(MPA)等多种类型,若不及时治疗,可能导致肾衰竭、呼吸衰竭等严重后果。近年来,随着生物制剂的发展,利妥昔单抗(RTX)作为一种创新的B细胞耗竭疗法,在AAV的治疗中展现出了显著的疗效。本文将深入解读RAVE研究,探讨利妥昔单抗在AAV治疗中的非劣效性。
RAVE研究背景
RAVE(Rituximab in ANCA-Associated Vasculitis)研究是一项多中心、随机、双盲、安慰剂对照的临床试验,旨在评估利妥昔单抗在AAV诱导缓解期的疗效和安全性。该研究由全球多个研究中心共同参与,纳入了大量新诊断或复发的AAV患者,为利妥昔单抗在AAV治疗中的应用提供了有力的证据。
研究设计与方法
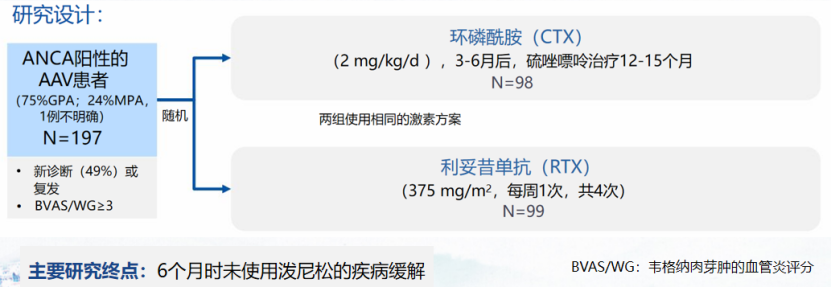
在RAVE研究中,患者被随机分配至利妥昔单抗组或环磷酰胺(CYC)组。利妥昔单抗组的患者接受每周一次、共四次、每次375mg/m²剂量的静脉滴注,同时接受糖皮质激素治疗。CYC组的患者则接受口服CYC和糖皮质激素治疗。研究的主要终点是在治疗6个月时达到疾病缓解的患者比例。
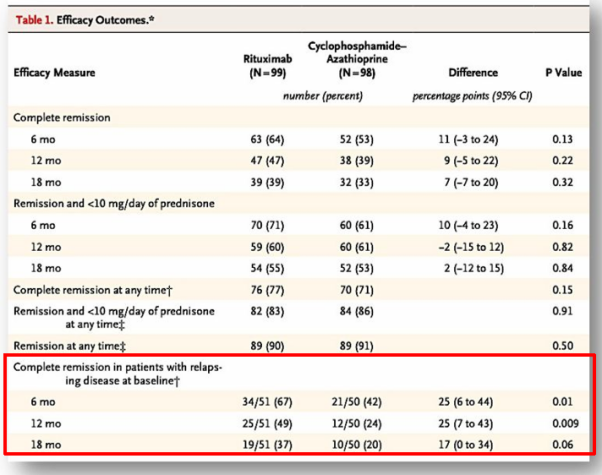
研究结果
RAVE研究的结果显示,利妥昔单抗在诱导AAV缓解方面与环磷酰胺具有非劣效性。具体来说,利妥昔单抗组的患者在治疗6个月时达到疾病缓解的比例与CYC组相似,且两组在安全性方面也无显著差异。此外,利妥昔单抗在治疗复发性AAV方面也表现出优于CYC的潜力,尤其是在长期随访中,利妥昔单抗能够显著降低疾病的复发率。
利妥昔单抗的作用机制与优势
利妥昔单抗是一种针对B细胞表面抗原CD20的人鼠嵌合型单抗隆抗体,其作用机制主要通过耗竭B细胞来实现。B细胞在AAV的发病机制中起着重要作用,它们能够产生针对自身抗原的抗体,从而引发血管壁的炎症反应。利妥昔单抗通过靶向并破坏B细胞,能够显著降低自身抗体的产生,从而减轻炎症反应,达到治疗AAV的目的。
与传统的CYC治疗相比,利妥昔单抗具有多种优势。首先,利妥昔单抗的给药方式更为简便,患者只需接受静脉滴注即可,无需长期口服药物。其次,利妥昔单抗的副作用相对较少,且多为轻度至中度,如恶心、皮疹等,而CYC则可能导致严重的骨髓抑制、感染等副作用。此外,利妥昔单抗在治疗复发性AAV方面也表现出更好的疗效,能够显著降低疾病的复发率,提高患者的生活质量。
展望与未来研究方向
尽管RAVE研究已经证实了利妥昔单抗在AAV治疗中的非劣效性,但未来的研究仍需进一步探索利妥昔单抗的最佳使用剂量、持续时间以及在不同患者群体中的疗效。此外,随着新型生物制剂的不断涌现,如补体抑制剂等,未来的AAV治疗将更加多样化,为患者提供更多的治疗选择。
总之,RAVE研究为利妥昔单抗在AAV治疗中的应用提供了有力的证据,推动了该领域的发展。随着研究的不断深入和新型生物制剂的出现,相信未来AAV的治疗将更加精准、有效,为患者带来更好的预后和生活质量。