糖皮质激素治疗是免疫性血小板减少症(ITP)治疗的基础。除此之外,随着对ITP病理生理机制的深入研究,针对不同靶点的新药物及不同类型药物的联合治疗不断更新,并在临床广泛应用。目前,ITP治疗方案明显增多,延长了初诊患者的缓解时间,提高了难治性患者的缓解率,然而仍有较多临床难题亟需解决。本期,邀请到华中科技大学同济医学院附属协和医院梅恒教授,分享目前ITP的治疗进展与挑战。
减少出血、维持血小板计数和改善生活质量是医患双方一致追寻的三大目标。研究显示,血小板计数与ITP患者的出血风险呈负相关性,尤其是伴严重出血的ITP患者死亡风险增加2.6倍。这表明,血小板计数越低ITP患者器官出血风险越高,进而增加死亡风险。同时,低血小板计数还会严重影响患者的身心健康,诱发焦虑、疲劳。
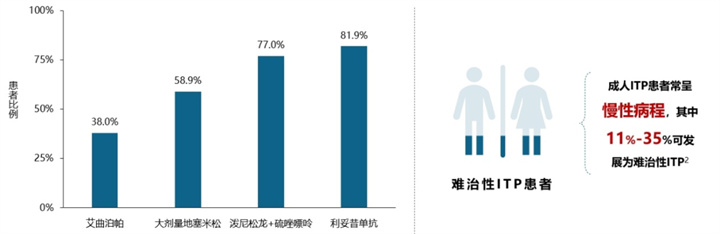
然而,即便经过一线/二线治疗,仍有部分ITP患者治疗失败,血小板计数难以恢复至安全范围:复发患者比例达到38%-82%,难治比例可达11%-35%。
此外,ITP患者合并症发生率高于非ITP患者,易合并糖尿病、白内障、肾衰竭等疾病,治疗复杂程度与治疗难度均进一步增加;并且因需要长期治疗,经济负担沉重。梅恒教授总结ITP治疗挑战表示,低血小板计数可导致ITP患者的出血、死亡风险增加,而即使经过规范化治疗,仍有部分患者治疗效果不佳,出现复发或进展为难治性ITP。
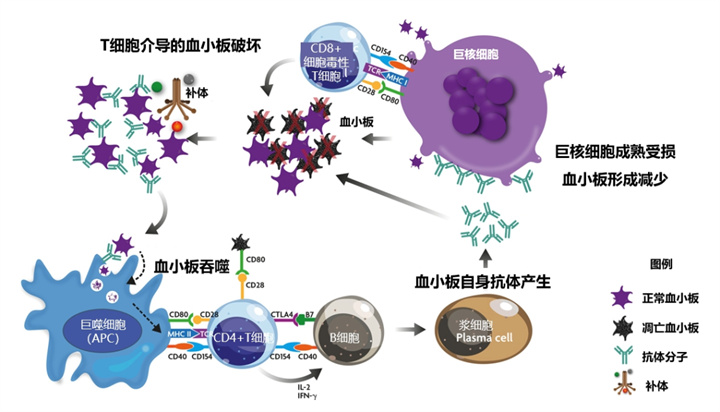
ITP主要发病机制是血小板自身抗原免疫耐受性丢失,导致B细胞和T细胞免疫异常活化,共同介导血小板破坏增加以及巨核细胞产生不足。
基于上述机制,ITP治疗应考虑标本兼治,既需要促进血小板生成,又需要减少血小板破坏。但目前绝大多数ITP治疗药物难以实现促进生成和减少破坏的双重作用。ITP相关治疗药物包括:
●减少血小板破坏:糖皮质激素、免疫球蛋白、利妥昔单抗、FcRn拮抗剂(艾加莫德、洛利昔珠单抗等)、Syk抑制剂(福坦替尼、索乐匹尼布等)、BTK抑制剂(利扎鲁替尼等)
●促进血小板生成:rhTPO、罗普司亭、艾曲泊帕、海曲泊帕、阿伐曲泊帕、芦曲泊帕
其中,最新获批的长效TPO-RA罗普司亭因独特的分子结构,既能有效提升ITP患者的血小板计数,又能降低抗体水平,效果瞩目。
综合国际共识及中国指南,ITP治疗目标为:①提升血小板达到安全水平;②减少出血事件;③不良反应最小化;④提高生活质量。
对于ITP的全程管理,梅恒教授表示有以下挑战亟待突破:
①重症ITP患者的紧急治疗,需要迅速升板的治疗药物。有研究提示,rhTPO的早期应答率优于艾曲泊帕;罗普司亭的早期应答率也优于艾曲泊帕。
②TPO/TPO-RA的合理转换。对于一种TPO-RA治疗无效的患者,可进行另一种TPO-RA转换治疗。从机制上来考虑,转换治疗应优先考虑作用位点不同的药物,再考虑位点相同的药物。
③确保长期用药安全性。对于肝功能受损的ITP患者,临床治疗过程中需选择肝脏安全性良好的药物。
④共病患者的多重用药。共病ITP患者由于多重用药的问题,临床需要选择药物相互作用(DDI)风险更低的药物。
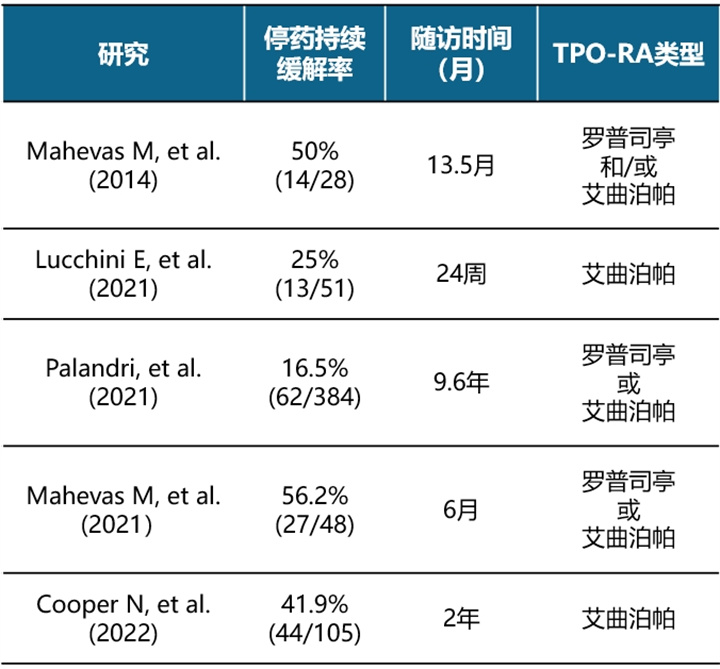
⑤实现无治疗缓解。多项临床研究证实,部分TPO-RA停药后可实现无治疗缓解。
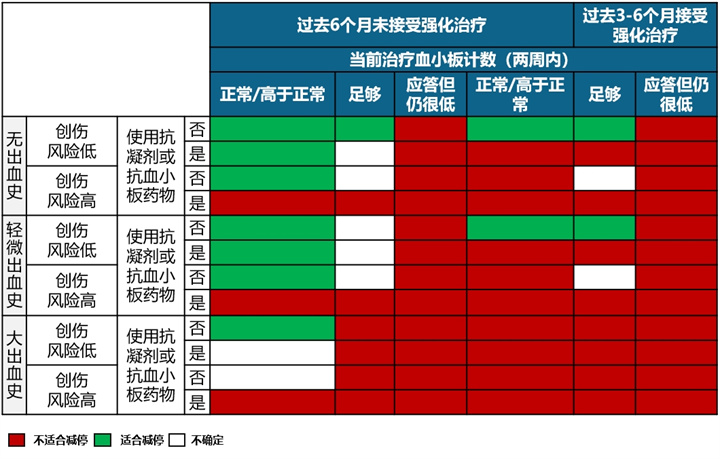
2020国际共识建议,TPO-RA治疗达稳态6个月后进行停药评估。可以考虑减停 TPO-RA 单药治疗的时机:
●血小板计数正常或高于正常值(>150×109/L),无大出血史,且在过去6个月无需接受强化治疗。
●血小板计数正常或高于正常值(>150×109/L),无大出血史,且在过去3-6个月需接受强化治疗,只要创伤风险低,未接受抗凝剂或抗血小板药物。
●血小板计数正常或高于正常值(>150×109/L),且有大出血史,只要创伤风险低,未使用抗凝剂或抗血小板药物,且在过去6个月内无需强化治疗。
●血小板计数低于正常水平但仍足够(50-150×109/L),只要无出血史,过去的6个月无需强化治疗,创伤风险低,未使用抗凝剂或抗血小板药物。
⑥降低患者治疗负担。ITP患者的经济负担沉重,在长期管理中应考虑治疗性价比高的治疗药物。
近几十年来,ITP治疗中,糖皮质激素作为一线治疗药物的地位暂未改变。虽然早期反应率高,但难以完全缓解或持续缓解,最终都会进展为慢性ITP,且药物不良反应多。ITP发病机制十分复杂,涉及免疫应答的各个环节,并非单一因素所致,由机制延伸的各种新型药物成为临床管理的重要“武器”,为患者提供了精准、有效的治疗。期待新型药物不断涌现,为广大患者带来康复的福音。