认识药物 | 佐来曲替尼:给“TRK融合肉瘤”按下暂停键的国产自研二代靶向药
但在肉瘤这个“大家族”里,有一小撮患者的肿瘤背后,藏着一个非常明确的“电门开关”——NTRK融合。一旦抓住它,疗效往往会出现“跳级式”的改变[1,2]。
而佐来曲替尼,就是围绕这个开关打造的二代TRK靶向药。
先搞懂:NTRK融合=
把“生长油门”焊死了
但当NTRK与别的基因“拼接融合”,就可能造出一个永远处于“开机状态”的异常TRK蛋白——相当于把细胞生长的油门焊死,肿瘤就会被持续驱动着往前冲[1,2]。
在肉瘤里,NTRK融合并不是“普遍存在”,但在某些亚型里非常高:
- 婴儿纤维肉瘤(infantilefibrosarcoma):NTRK融合可见于>90%病例,是典型“对靶点高度依赖”的那类肿瘤[1]。
- 在更广泛的软组织肉瘤人群中,NTRK融合总体比例较低,但研究里也观察到例如软组织肉瘤约3%、纤维肉瘤亚型更高(可到两位数)这样的分布[3]。
二代TRK抑制剂
那它是怎么起作用的呢?[4,5]
可以把佐来曲替尼想成:专门去堵TRK信号通路的“总闸门”。它是高选择性的泛TRK抑制剂,覆盖TRKA/TRKB/TRKC。
为什么说它是“二代”?
很多一代TRK抑制剂(如拉罗替尼、恩曲替尼)已经能带来很好的缓解,但临床里仍会遇到两类“卡点”[3,5]:
- 耐药突变:肿瘤在药物压力下进化,TRK激酶位点出现“溶剂前沿”等突变,让一代药“卡不进去”。
- 脑部病灶:需要药物能更好穿过血脑屏障。
佐来曲替尼的设计目标之一,就是在这些点上“更进一步”:[3-5]
- 前临床研究显示它对多种一代TRK抑制剂耐药突变仍保持活性,并在脑穿透相关指标上表现更强。
- 公司公布的注册研究也强调其透脑活性与对一代耐药后的潜在作用。
而是“NTRK融合”
佐来曲替尼的逻辑是“看基因,不看瘤种”(肿瘤驱动基因一致,就可能受益)。它在中国获批适应证也是按“携带NTRK融合基因的实体瘤”来描述,而不是限定某个癌种。
换句话说:
- 你是骨肉瘤/脂肪肉瘤/滑膜肉瘤……都不重要;
- 重要的是:你有没有NTRK融合(NTRK1/2/3任一融合)。
(肉瘤患者自查清单)
✅诊断为肉瘤(尤其是某些更容易出现NTRK融合的亚型/形态学提示);
✅通过可靠检测证实NTRK基因融合阳性(NTRK1/2/3);
✅局部晚期/转移,或标准治疗后仍进展;
✅年龄满足已获批人群:在中国为≥12岁青少年及成人(儿童更小年龄段仍在推进注册研究)。
加分项(但不是必须):
既往用过一代TRK抑制剂后出现耐药,医生在评估耐药机制后,可能会讨论二代药的意义。
疗效到底有多“能打”?
(《临床肿瘤学杂志》
2025年会摘要)
截至2024-11-23:两项试验共入组229名成人;其中49名“未用过TRK抑制剂”的成人可评估疗效,覆盖12种肿瘤类型。
- 确认客观缓解率83.7%(95%置信区间70.3–92.7),其中完全缓解10.2%。
- 缓解持续时间和无进展生存期的中位数均尚未达到;12个月缓解持续率92.0%、12个月无进展生存率90.5%。
- 基线伴脑转移的3人里,2人出现颅内缓解。
(《临床肿瘤学杂志》
2025年会摘要)
截至2024-11-23:共入组18人;其中6名“未用过TRK抑制剂且中央实验室确认TRK融合阳性”可评估疗效。
- 确认客观缓解率100%(95%置信区间54.1–100),且首次评估均为部分缓解并在截点时维持。
- 中位起效时间约1个月(青少年1.0月;儿童0.9月)。
- 值得注意:摘要里提到1位儿童在一代TRK抑制剂进展后,换用佐来曲替尼达到完全缓解。
一代TRK抑制剂
在TRK融合肉瘤里也确实很强
这不是在岔题,而是帮你校准“TRK这条线到底值不值得追”。在一项成人TRK融合肉瘤的扩展分析中,拉罗替尼在该人群的客观缓解率为58%,并强调反应持久与安全性良好。
为什么要提这一段?因为它说明:TRK融合在肉瘤里一旦命中,是“能改变局面”的靶点;而二代药(包括佐来曲替尼)则被寄希望于把“耐药与颅内”这些短板补上。
用“硬数据”说话[4,6]
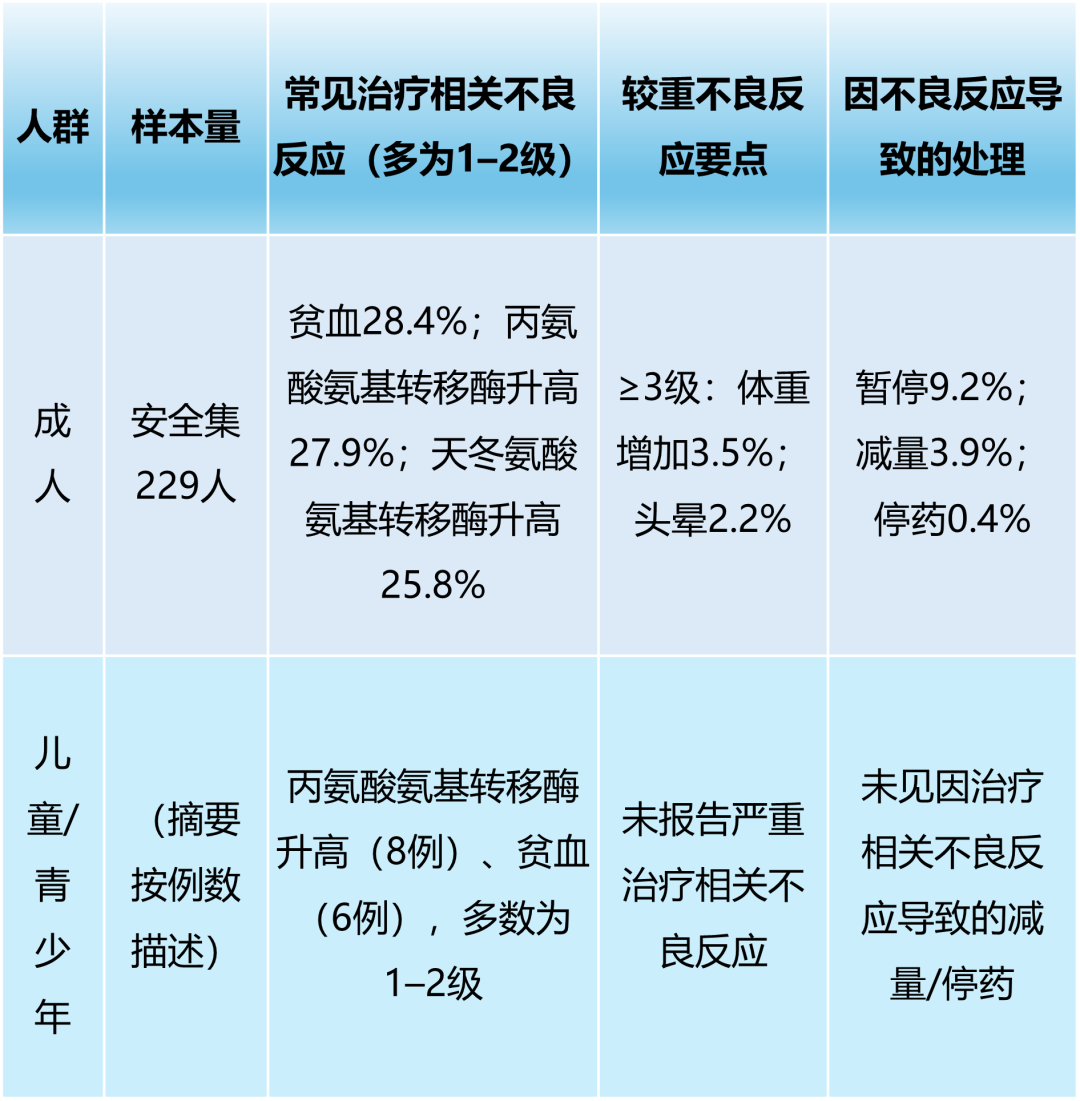
- 贫血/肝酶升高这些,通常靠“抽血监测+需要时调整”就能管住;
- 如果出现明显头晕,先把“开车/爬楼/独自外出”按暂停键,及时告诉医生;
- 体重增加不是“你不自律”,它可能是药物相关信号之一(摘要里确实出现了≥3级体重增加)。
咨询和交流肉瘤(sarcoma)相关问题


